이글의 목차
농도 중 %농도는 알겠는데, mol 농도, PPM, PPB는 뭐지?
1. 화학 농도, 왜 이렇게 복잡할까?
뉴스 등에서 “○○지역 미세먼지 농도가 150㎍/㎥를 넘어섰다”등의 내용을 한 번 들으신 기억이 있을 겁니다. 또 마트에서 생수를 사려고 보니 “미네랄 함량 50ppm”이라고 적혀 있는 것 도 보신 적 있을 겁니다. 그리고 학교에서 화학 시간에는 “0.1M 황산 용액”이라는 표현을 쓰고… 도대체 이 농도 단위들은 다 뭐가 다른 걸까요?
사실 저도 처음엔 %농도만 알았어요. 소금물의 농도가 3%라고 하면 100g 중에 3g이 소금이구나 하고 쉽게 이해했죠. 그런데 화학을 더 깊이 공부하다 보니 몰농도, 백만분율, 십억분율 같은 생소한 단위들이 튀어나오더라고요. 오늘은 이런 농도 단위들을 여러분과 함께 차근차근 알아보려고 합니다.
여러분도 혹시 실험실에서 시약을 만들거나, 수질 검사 결과를 보면서 이런 단위들 때문에 헷갈리신 적 있으신가요? 걱정 마세요. 이 글을 다 읽고 나면 mol 농도가 뭔지, PPM과 PPB가 어떻게 다른지 확실히 구분할 수 있게 될 거예요.
2. mol 농도(몰농도) – 화학자들의 필수 단위
먼저 mol 농도부터 알아볼까요? 화학을 전공한 친구가 있다면 아마 이 단위를 가장 많이 쓸 거예요. mol 농도는 용액 1리터에 녹아 있는 용질의 몰수를 나타내는 단위입니다. 단위는 M(몰라) 또는 mol/L로 표시하죠.
자, 여기서 잠깐! ‘몰(mol)’이라는 게 뭔지 모르시는 분들을 위해 쉽게 설명해드릴게요. 몰은 원자나 분자를 세는 단위인데, 마치 계란을 ‘판’으로 세는 것과 비슷해요. 계란 30개를 한 판이라고 하듯이, 분자 6.022×10²³개를 1몰이라고 부르는 거죠. 이 숫자가 엄청나게 크죠? 그래서 실제로 우리가 다루는 물질의 양과 잘 맞아떨어진답니다.
예를 들어볼까요? 소금(NaCl)의 분자량이 58.44g/mol이라고 하면, 1M NaCl 용액은 1리터에 소금 58.44g이 녹아 있는 용액이에요. 만약 0.5M 용액을 만들고 싶다면? 절반인 29.22g만 녹이면 되는 거죠. 참 간단하지 않나요?
실험실에서 일하는 제 조카가 말하길, mol 농도를 쓰는 가장 큰 이유는 화학 반응을 계산하기 편해서래요. 화학 반응은 분자 개수의 비율로 일어나니까, 몰 농도를 알면 반응에 필요한 정확한 양을 계산할 수 있거든요. 예를 들어 중화 반응에서 1M 염산 100mL와 완전히 반응하려면 1M 수산화나트륨이 정확히 100mL 필요하다는 걸 바로 알 수 있죠.
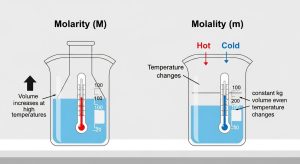
하지만 mol 농도에도 단점이 있어요. 온도가 변하면 용액의 부피가 변해서 농도도 달라진다는 거예요. 여름에 만든 용액이 겨울에는 농도가 살짝 달라질 수 있다는 뜻이죠. 그래서 정밀한 실험에서는 온도를 일정하게 유지하거나, 아예 온도 영향을 받지 않는 몰랄 농도를 쓰기도 한답니다.
3. 몰랄농도 – 온도 변화에도 끄떡없는 농도
앞서 몰농도의 단점으로 온도 변화에 따른 농도 변화를 언급했죠? 이 문제를 해결하기 위해 등장한 것이 바로 몰랄농도입니다. 몰랄농도는 용매 1kg에 녹아 있는 용질의 몰수를 나타내는 단위예요. 단위는 m 또는 mol/kg으로 표시합니다.
여기서 주의할 점! 몰농도는 ‘용액’ 1리터를 기준으로 하지만, 몰랄농도는 ‘용매’ 1kg을 기준으로 한다는 거예요. 예를 들어 설명해볼게요. 물 1kg(1000g)에 소금 58.44g(1몰)을 녹이면, 이 용액의 몰랄농도는 1m(1 mol/kg)이 됩니다.
“그런데 왜 굳이 용매의 질량을 쓰는 거죠?” 라고 물으실 수 있어요. 바로 질량은 온도나 압력이 변해도 변하지 않기 때문이에요! 물 1kg은 영하 10도에서도, 영상 40도에서도 여전히 1kg이죠. 반면 부피는 온도에 따라 팽창하거나 수축하잖아요. 그래서 정밀한 실험, 특히 끓는점 오름이나 어는점 내림 같은 용액의 총괄성을 연구할 때는 몰랄농도를 사용한답니다.
실제로 겨울철 도로에 뿌리는 제설용 염화칼슘의 효과를 계산할 때도 몰랄농도를 써요. 어는점 내림 공식(ΔT = Kf × m × i)에서 m이 바로 몰랄농도거든요. 염화칼슘 1몰랄 용액은 물의 어는점을 약 5.58도 낮춰서 영하 5.58도까지 얼지 않게 만듭니다.
몰농도와 몰랄농도, 이름도 비슷하고 헷갈리시죠? 영어로도 Molarity와 Molality로 정말 비슷해요. 처음 화학을 배우는 학생들이 가장 헷갈려하는 부분 중 하나랍니다. 간단히 정리하면:
- 몰농도(M) = 용질의 몰수 ÷ 용액의 부피(L)
- 몰랄농도(m) = 용질의 몰수 ÷ 용매의 질량(kg)
화학 교수님이 농담으로 하신 말씀이 생각나네요. “몰농도는 M으로 쓰고 몰라(Molar)라고 읽고, 몰랄농도는 m으로 쓰고 몰랄(molal)이라고 읽는데, 둘 다 몰라서 문제야!” 라고요. 하지만 이제 여러분은 확실히 구분할 수 있겠죠?
4. PPM이란? – 100만분의 1의 세계
이번엔 백만분율에 대해 알아볼 차례예요. PPM은 ‘Parts Per Million’의 약자로, 우리말로는 ‘백만분율’이라고 부릅니다. 100만분의 1을 나타내는 단위죠.
이 단위를 이해하기 쉽게 설명하면, 물 1톤(1,000kg = 1,000,000g)에 어떤 물질 1g이 녹아 있으면 그게 바로 1ppm이에요. 물의 비중이 1이라고 가정하면, 1리터(1000mL)에 1mg이 녹아 있는 것도 백만분의 1이 됩니다. 그래서 수질 분석에서는 보통 이 단위를 mg/L로 쓰이죠.
좀 더 와닿는 예를 들어볼까요? 집에 있는 욕조에 물을 가득 채우면 대략 300리터 정도 됩니다. 여기에 잉크를 6방울(약 0.3mL) 떨어뜨렸다고 생각해보세요. 그 정도의 농도가 바로 1ppm이에요. 정말 적은 양이죠?
PPM은 주로 어디에 쓰일까요? 우리 주변에서 정말 많이 쓰입니다! 대기 중 이산화탄소 농도(현재 약 420ppm), 수돗물의 잔류 염소 농도(보통 0.2~0.4ppm), 지하수의 중금속 함량, 심지어 금광석의 금 함량도 PPM으로 표시해요. 농약 잔류량 검사에서도 자주 볼 수 있는 단위죠.
재미있는 사실 하나 알려드릴까요? 우리가 마시는 생수에 표시된 미네랄 함량도 대부분 ppm 단위예요. “칼슘 50ppm”이라고 쓰여 있다면, 1리터에 칼슘이 50mg 들어있다는 뜻이랍니다. 이제 생수병 라벨을 볼 때마다 그 의미를 정확히 알 수 있겠죠?
PPM의 장점은 온도나 압력이 변해도 질량비는 변하지 않기 때문에 안정적이라는 거예요. 하지만 기체의 경우는 좀 달라요. 기체는 온도와 압력에 따라 부피가 크게 변하기 때문에, 보통 25℃, 1기압을 표준 상태로 정해놓고 측정한답니다.
5. PPB는 뭐가 다른가? – 더 작은 농도를 측정하는 법
PPM보다 더 작은 농도를 측정해야 할 때는 어떻게 할까요? 바로 PPB를 사용합니다! PPB는 ‘Parts Per Billion’의 약자로, 10억분의 1을 나타내요. PPM보다 1000배 더 작은 단위죠. 쉽게 말해서 1ppm = 1000ppb입니다.
PPB를 실감나게 설명하면 이렇습니다. 올림픽 규격 수영장(길이 50m, 폭 25m, 깊이 2m)에 물을 가득 채우면 약 2500톤이 됩니다. 여기에 각설탕 한 개(약 2.5g)를 녹이면 대략 1ppb가 되는 거예요. 정말 극소량이죠?
언제 PPB를 쓸까요? 주로 아주 미량의 오염물질을 측정할 때 사용해요. 예를 들어 반도체 공장의 초순수(울트라 퓨어 워터)는 불순물이 ppb 단위로 관리됩니다. 식품의 중금속 오염도 측정할 때도 ppb를 쓰고요. 최근에는 환경호르몬이나 의약품 잔류물질 같은 극미량 오염물질을 측정할 때 자주 사용된답니다.
실제로 우리나라 먹는 물 수질 기준을 보면, 수은은 1ppb(0.001ppm) 이하, 납은 10ppb(0.01ppm) 이하로 정해져 있어요. 이렇게 작은 양도 우리 건강에 영향을 줄 수 있기 때문에 엄격하게 관리하는 거죠.
여기서 많은 분들이 헷갈려하는 부분이 있어요. “그럼 PPT(Parts Per Trillion, 1조분의 1)도 있나요?”라고 물으시는데, 네, 있습니다! 하지만 일반적으로는 거의 사용하지 않아요. 왜냐하면 그 정도로 미량을 측정하는 기술 자체가 매우 어렵고, 실용적인 의미도 크지 않거든요.
6. 실생활에서 만나는 농도 단위들
이제 이런 농도 단위들이 우리 일상생활에서 어떻게 쓰이는지 구체적으로 알아볼까요?
병원에서 링거를 맞아보신 적 있으신가요? 포도당 주사액이나 생리식염수 같은 수액에는 mol 농도가 표시되어 있어요. 예를 들어 5% 포도당 용액은 약 0.28M 정도 되고, 0.9% 생리식염수는 약 0.15M이에요. 의사들이 환자의 상태에 따라 적절한 농도의 수액을 선택하는 거죠.
겨울철 자동차 부동액을 넣어보신 적 있나요? 부동액의 농도를 계산할 때는 몰랄농도를 사용해요. 에틸렌글리콜 수용액의 몰랄농도가 높을수록 어는점이 더 많이 내려가거든요. 보통 50% 부동액(약 16몰랄)을 사용하면 영하 37도까지 얼지 않는답니다. 제설용 염화칼슘도 마찬가지예요. 도로에 뿌린 염화칼슘이 눈을 녹이는 원리도 몰랄농도와 관련이 있죠.
수영장 물 관리하시는 분들은 PPM을 자주 접하실 거예요. 수영장의 염소 농도는 보통 1~3ppm으로 유지해야 합니다. 너무 낮으면 살균 효과가 떨어지고, 너무 높으면 피부나 눈이 따가워요. pH 조절제나 알칼리도 조절제의 사용량도 모두 ppm 단위로 계산한답니다.
농사짓는 분들도 이런 단위를 자주 사용해요. 비료의 농도를 조절할 때 PPM을 쓰거든요. 예를 들어 수경재배에서는 양액의 농도를 EC(전기전도도)로 측정하는데, 이것도 결국 PPM으로 환산할 수 있어요. 토마토는 보통 20002500ppm, 상추는 10001500ppm 정도의 양액 농도가 적당하다고 해요.
최근 이슈가 되는 미세먼지 농도는 어떨까요? 미세먼지는 ㎍/㎥(마이크로그램 퍼 큐빅미터) 단위를 주로 쓰지만, 가스상 오염물질인 오존이나 이산화황 같은 경우는 ppm이나 ppb로 표시하기도 해요. 예를 들어 오존주의보는 오존 농도가 0.12ppm(120ppb) 이상일 때 발령된답니다.
7. 농도 단위 간 변환하기
자, 이제 각 농도 단위가 뭔지는 알았는데, 서로 변환하는 건 어떻게 할까요? 이 부분이 많은 분들이 어려워하시는 부분이에요.
먼저 가장 간단한 PPM과 PPB 변환부터 해볼까요?
- 1 ppm = 1000 ppb
- 1 ppb = 0.001 ppm
예를 들어, 5ppm을 ppb로 바꾸면? 5 × 1000 = 5000ppb가 되는 거죠. 반대로 300ppb를 ppm으로 바꾸면? 300 ÷ 1000 = 0.3ppm이 됩니다.
퍼센트 농도와 PPM의 관계는 어떨까요?
- 1% = 10,000 ppm
- 1 ppm = 0.0001%
그래서 0.05% 농도는 500ppm이 되는 거예요.
mol 농도를 PPM으로 바꾸는 건 좀 복잡해요. 용질의 분자량을 알아야 하거든요. 공식은 이렇습니다: ppm = 몰농도(M) × 분자량(g/mol) × 1000
예를 들어, 0.01M 소금(NaCl, 분자량 58.44) 용액은? 0.01 × 58.44 × 1000 = 584.4 ppm이 됩니다.
몰농도와 몰랄농도 사이의 변환은 어떨까요? 이건 용액의 밀도를 알아야 해요. 묽은 수용액(밀도가 거의 1g/mL)의 경우, 몰농도와 몰랄농도가 거의 비슷합니다. 하지만 진한 용액에서는 차이가 커져요.
예를 들어, 1M 설탕물(분자량 342)의 몰랄농도를 구하려면:
- 1L 용액에 설탕 342g이 들어있음
- 용액의 밀도가 약 1.13g/mL라면, 용액 1L의 질량은 1130g
- 물의 질량 = 1130 – 342 = 788g = 0.788kg
- 몰랄농도 = 1몰 ÷ 0.788kg = 1.27m
보시다시피 농도가 진해질수록 몰농도와 몰랄농도의 차이가 커집니다.
하지만 걱정하지 마세요! 요즘은 온라인 농도 계산기나 스마트폰 앱으로 쉽게 변환할 수 있어요. 실험실에서 일하는 분들은 보통 엑셀 시트에 공식을 저장해놓고 사용한답니다.
8. 흔한 오해와 진실
농도 단위에 대해 많은 분들이 오해하는 부분들을 짚어볼게요.
오해 1: “몰농도와 몰랄농도는 같은 거 아닌가?” 진실: 전혀 달라요! 몰농도는 용액의 부피 기준, 몰랄농도는 용매의 질량 기준입니다. 묽은 수용액에서는 비슷한 값이 나오지만, 진한 용액에서는 큰 차이가 납니다.
오해 2: “PPM은 항상 mg/L와 같다” 진실: 물처럼 비중이 1인 용액에서만 그래요. 비중이 다른 용액에서는 달라집니다. 예를 들어 비중이 1.5인 용액에서 1ppm은 1.5mg/L가 되죠.
오해 3: “mol 농도가 높으면 무조건 진한 용액이다” 진실: 꼭 그렇지는 않아요. 분자량이 작은 물질은 같은 몰농도에서도 실제 질량은 적거든요. 1M 염산(분자량 36.5)보다 1M 설탕물(분자량 342)이 훨씬 많은 양의 용질을 포함하고 있어요.
오해 4: “PPB는 너무 작아서 무시해도 된다” 진실: 절대 그렇지 않아요! 어떤 물질은 ppb 수준에서도 큰 영향을 미칩니다. 예를 들어 다이옥신 같은 물질은 ppt(1조분의 1) 수준에서도 위험할 수 있어요.
오해 5: “농도가 낮으면 안전하다” 진실: 물질의 독성에 따라 달라요. 청산가리는 ppm 수준에서도 치명적이지만, 소금은 수천 ppm이어도 큰 문제가 없죠. 중요한 건 농도 자체가 아니라 그 물질의 특성과 농도를 함께 고려하는 거예요.
오해 6: “모든 나라가 같은 농도 기준을 사용한다” 진실: 대부분 비슷하지만, 나라마다 조금씩 달라요. 특히 환경 기준이나 식품 안전 기준은 각 나라의 상황에 따라 다르게 정해집니다. 그래서 국제 거래를 할 때는 어느 나라 기준을 따를지 명확히 해야 해요.
9. 마무리하며
오늘 우리는 %농도 외에도 화학에서 자주 사용되는 mol 농도, 몰랄농도, PPM, PPB에 대해 자세히 알아봤습니다. mol 농도는 화학 반응을 계산할 때 편리하고, 몰랄농도는 온도 변화에 영향받지 않아 정밀한 실험에 유용하며, PPM과 PPB는 미량의 물질을 측정할 때 필수적이라는 걸 배웠죠.
처음엔 복잡해 보였지만, 각각의 용도와 의미를 이해하니 그리 어렵지 않죠? 이제 뉴스에서 “수돗물의 잔류 염소 농도가 0.3ppm”이라고 하면, “아, 1톤의 물에 0.3g의 염소가 있구나”라고 바로 이해할 수 있을 거예요.
농도 단위는 단순한 숫자가 아니라 우리 생활과 건강, 환경을 지키는 중요한 도구입니다. 수질을 관리하고, 약품을 만들고, 환경을 모니터링하는 데 꼭 필요하죠. 여러분도 이제 이런 단위들을 만날 때마다 좀 더 친숙하게 느끼실 수 있기를 바랍니다.
혹시 실험을 하거나 관련 일을 하시는 분들은 항상 정확한 농도 계산을 하시길 바라요. 작은 실수가 큰 차이를 만들 수 있으니까요. 그리고 일반인 분들도 이제는 제품 라벨이나 검사 결과를 볼 때 그 숫자들이 의미하는 바를 정확히 이해하실 수 있을 거예요.