이글의 목차
이온결합, 공유결합, 금속결합이란?
목차
- 서론 – 원자들의 만남, 그 특별한 이야기
- 이온결합 – 전자를 주고받는 극적인 만남
- 공유결합 – 전자를 나누는 평화로운 동거
- 금속결합 – 전자의 바다를 헤엄치는 자유로운 영혼들
- 세 가지 결합의 차이점과 특성 비교
- 일상생활에서 만나는 화학결합의 예시들
- 결론 – 우리 주변의 모든 것이 화학결합의 결과물
1. 서론 – 원자들의 만남, 그 특별한 이야기
여러분은 혹시 소금을 먹으면서 “이 하얀 결정이 어떻게 만들어졌을까?” 하고 궁금해해본 적이 있으신가요? 아니면 반지를 끼면서 “이 금속이 왜 이렇게 반짝이고 단단할까?” 생각해보신 적은요? 저는 고등학생 때 화학 시간에 처음으로 이런 질문을 던졌던 기억이 납니다. 선생님께서는 웃으시며 “그게 바로 화학결합의 마법이야”라고 말씀하셨죠.
우리가 살아가는 세상의 모든 물질은 원자들이 서로 손을 잡고 만들어낸 작품입니다. 마치 사람들이 서로 다른 방식으로 관계를 맺듯이, 원자들도 각자의 방식으로 결합을 이루며 다양한 물질을 만들어냅니다. 어떤 원자들은 전자를 완전히 주고받으며 극적인 만남을 갖고, 어떤 원자들은 전자를 사이좋게 나누며 평화로운 동거를 시작하고, 또 어떤 원자들은 전자의 바다를 만들어 그 안에서 자유롭게 헤엄치며 살아갑니다.
이런 원자들의 만남 방식을 우리는 화학결합이라고 부릅니다. 그리고 그 중에서도 가장 중요한 세 가지가 바로 이온결합, 공유결합, 그리고 금속결합입니다. 오늘은 이 세 가지 결합이 어떻게 다르고, 왜 그런 차이가 생기는지, 그리고 우리 일상생활과 어떤 관련이 있는지 재미있게 풀어드리겠습니다.
2. 이온결합 – 전자를 주고받는 극적인 만남
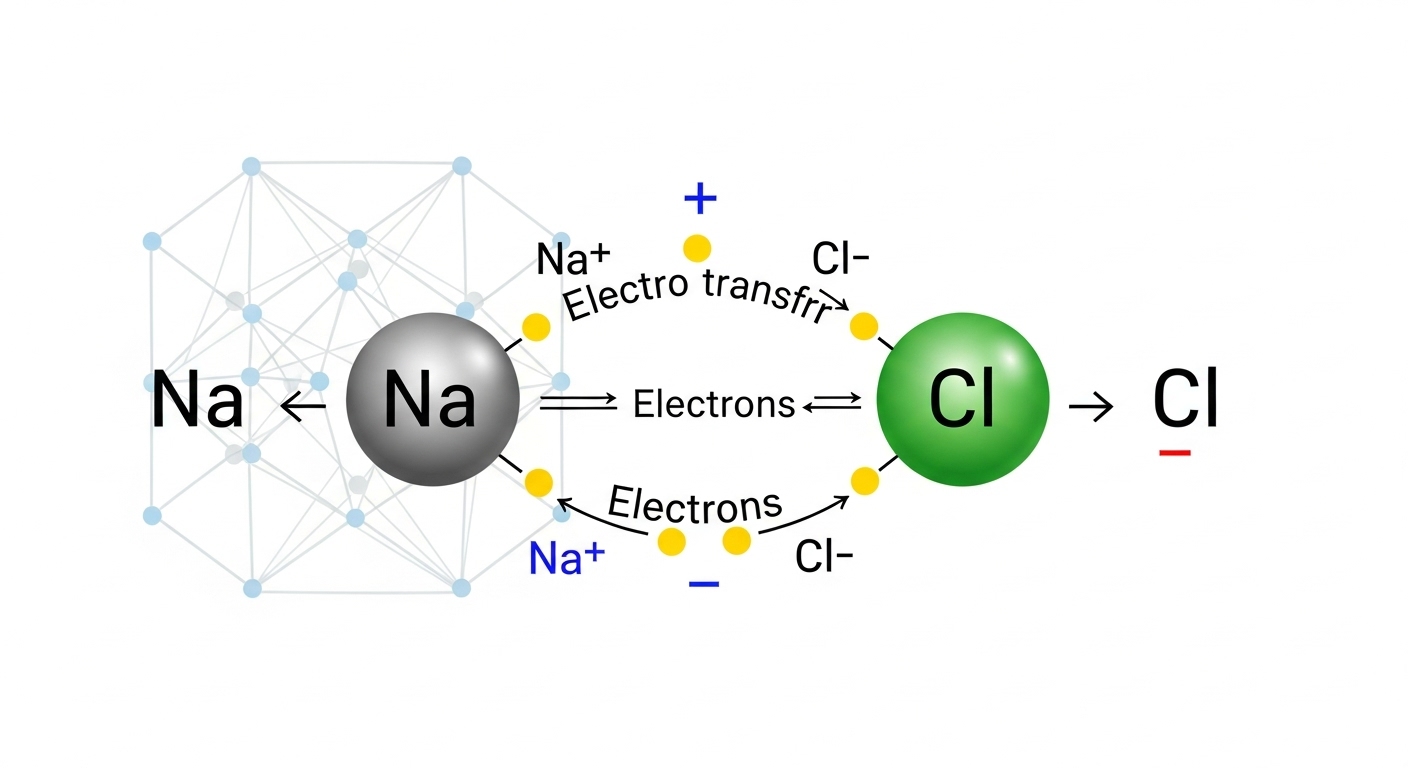
이온결합을 설명할 때 저는 항상 로미오와 줄리엣 같은 극적인 사랑 이야기를 떠올립니다. 하지만 여기서는 사랑 대신 전자가 주인공이죠. 금속 원자는 자신이 가진 전자를 비금속 원자에게 선뜻 내어주고, 비금속 원자는 그 전자를 감사히 받아들입니다. 이 과정에서 금속 원자는 양이온이 되고, 비금속 원자는 음이온이 됩니다.
이온결합은 금속과 비금속 사이에서 전자가 완전히 이동하여 형성되는 결합으로, 양이온과 음이온 사이의 정전기적 인력으로 만들어집니다. 가장 대표적인 예가 바로 우리가 매일 먹는 소금, 즉 염화나트륨(NaCl)입니다. 나트륨 원자는 전자 하나를 염소 원자에게 넘겨주고, 그 결과 Na+ 이온과 Cl- 이온이 만들어져 서로 강하게 끌어당기게 됩니다.
이렇게 형성된 이온결합 물질들은 매우 독특한 성질을 보입니다. 이온결합 물질은 높은 녹는점과 끓는점을 가지며, 고체 상태에서는 전기를 전도하지 않지만 물에 녹거나 액체 상태가 되면 전기를 전도합니다. 여러분이 소금물이 전기를 통하게 한다는 실험을 본 적이 있다면, 바로 이 원리 때문입니다. 고체 상태의 소금은 이온들이 격자 구조에 꽉 묶여 있어 움직일 수 없지만, 물에 녹으면 이온들이 자유롭게 움직이며 전기를 전달할 수 있게 되는 것입니다.
많은 사람들이 오해하는 부분이 있는데, 이온결합 물질을 ‘분자’라고 부르는 경우가 있습니다. 하지만 이는 틀린 표현입니다. 이온결합 물질은 이온들이 사방으로 결합하여 거대한 결정 구조를 이루기 때문에 분자라고 부르지 않습니다. 소금 결정 하나를 보면, 그 안에는 수많은 Na+ 이온과 Cl- 이온들이 규칙적으로 배열되어 있을 뿐, 독립적인 NaCl 분자가 존재하는 것은 아닙니다.
3. 공유결합 – 전자를 나누는 평화로운 동거
공유결합은 이온결합과는 완전히 다른 방식의 만남입니다. 만약 이온결합이 한쪽이 모든 것을 주고 다른 쪽이 받는 관계라면, 공유결합은 서로가 가진 것을 함께 나누며 살아가는 평등한 관계라고 할 수 있습니다. 공유결합은 주로 비금속 원자들 사이에서 일어나며, 원자들이 전자쌍을 공유하여 안정한 전자 배치를 이루는 결합입니다.
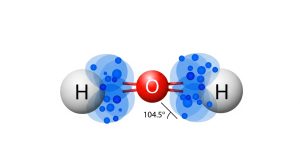
물(H2O)을 예로 들어보겠습니다. 수소 원자 두 개와 산소 원자 하나가 만날 때, 그들은 전자를 완전히 주고받는 대신 서로 공유하기로 결정합니다. 각 수소 원자는 자신의 전자 하나를 산소와 나누고, 산소도 자신의 전자를 수소와 나눕니다. 이렇게 해서 모든 원자가 안정한 전자 배치를 갖게 되는 것이죠.
공유결합의 재미있는 점은 전자를 공유하는 정도가 항상 똑같지 않다는 것입니다. 원자들의 전기음성도 차이에 따라 극성 공유결합과 무극성 공유결합으로 나뉩니다. 예를 들어, 염소 분자(Cl2)처럼 같은 원자끼리 결합하면 전자를 완벽하게 똑같이 나누는 무극성 공유결합이 되지만, 물 분자처럼 다른 원자끼리 결합하면 전자가 한쪽으로 조금 더 치우친 극성 공유결합이 됩니다.
공유결합 물질들은 일반적으로 이온결합 물질보다 낮은 녹는점과 끓는점을 가지며, 대부분 전기를 전도하지 않습니다. 설탕이 소금보다 쉽게 녹고, 설탕물이 전기를 통하지 않는 것도 바로 이 때문입니다. 공유결합 물질은 분자 단위로 존재하기 때문에 ‘분자’라는 말을 붙여 부를 수 있습니다. 우리가 숨 쉬는 산소 분자(O2), 질소 분자(N2) 모두 공유결합으로 이루어진 대표적인 예입니다.
여기서 잠깐, 다이아몬드 이야기를 해보겠습니다. 다이아몬드는 탄소 원자들이 공유결합으로 연결된 물질인데, 일반적인 공유결합 물질과는 다르게 엄청나게 단단합니다. 왜 그럴까요? 바로 탄소 원자 하나가 주변의 네 개 탄소 원자와 강한 공유결합을 만들며 3차원 네트워크 구조를 형성하기 때문입니다. 이런 특별한 구조를 ‘공유결합 결정’이라고 부르며, 일반적인 분자성 공유결합 물질과는 구별됩니다.

4. 금속결합 – 전자의 바다를 헤엄치는 자유로운 영혼들
금속결합은 앞의 두 결합과는 또 다른 독특한 방식입니다. 만약 이온결합이 극적인 사랑이고, 공유결합이 평화로운 동거라면, 금속결합은 자유로운 공동체 생활이라고 할 수 있겠네요. 금속결합에서는 금속 원자들이 최외각 전자를 내놓아 ‘전자의 바다’를 만들고, 양이온이 된 금속 원자들이 이 전자의 바다 속에서 함께 존재합니다.
구리 전선을 생각해보세요. 구리 원자들은 자신의 최외각 전자를 자유롭게 풀어놓고, 이 전자들은 구리 원자들 사이를 자유롭게 돌아다닙니다. 마치 바다처럼 말이죠. 이 전자의 바다가 바로 금속이 전기를 잘 전도하는 이유입니다. 전압을 걸면 이 자유전자들이 한 방향으로 흐르면서 전류가 되는 것입니다.
금속결합 물질은 높은 전기 전도성과 열 전도성을 가지며, 연성(늘어나는 성질)과 전성(펴지는 성질)이 있어 다양한 모양으로 가공할 수 있습니다. 금속을 두드리면 찌그러지지 않고 펴지는 이유도, 금속 원자층들이 서로 미끄러지면서도 전자의 바다가 계속 결합을 유지해주기 때문입니다. 반면 이온결합 물질인 소금을 두드리면 부서지죠. 이온들의 배열이 어긋나면서 같은 전하끼리 반발하기 때문입니다.
금속의 반짝이는 광택도 이 자유전자 때문입니다. 빛이 금속 표면에 닿으면 자유전자들이 빛을 흡수했다가 다시 방출하면서 특유의 금속 광택을 만들어냅니다. 그래서 금이나 은 같은 금속들이 그렇게 아름답게 빛나는 것이죠.
5. 세 가지 결합의 차이점과 특성 비교
이제 세 가지 화학결합의 차이점을 정리해보겠습니다. 각각의 결합은 형성되는 원리부터 물질의 성질까지 확연히 다른 특징을 보입니다.
먼저 결합이 일어나는 원소들을 보면, 이온결합은 주로 금속과 비금속 사이에서, 공유결합은 비금속과 비금속 사이에서, 그리고 금속결합은 금속과 금속 사이에서 일어납니다. 이는 원소들의 전기음성도와 이온화 에너지 차이 때문입니다. 금속은 전자를 잃기 쉽고, 비금속은 전자를 얻기 쉬운 성질이 있어서 이런 차이가 생기는 것이죠.
전기 전도성 측면에서도 큰 차이를 보입니다. 이온결합 물질은 고체 상태에서는 전기가 통하지 않지만 녹거나 물에 녹으면 전기가 통합니다. 공유결합 물질은 대부분 어떤 상태에서도 전기가 통하지 않습니다. 하지만 금속결합 물질은 항상 전기가 잘 통합니다. 이런 차이 때문에 전선은 구리나 알루미늄 같은 금속으로 만들고, 전선의 피복은 플라스틱 같은 공유결합 물질로 만드는 것입니다.
물리적 성질도 매우 다릅니다. 이온결합 물질은 단단하지만 부서지기 쉽고, 공유결합 물질은 다양한 형태(기체, 액체, 고체)로 존재하며, 금속결합 물질은 단단하면서도 유연합니다. 이런 특성 때문에 건축 자재로는 금속이 많이 사용되고, 포장재로는 플라스틱이 사용되며, 조미료로는 소금 같은 이온결합 물질이 사용되는 것입니다.
전반적으로 이온결합과 공유결합 물질은 높은 녹는점을 가질 수 있지만, 금속결합 물질의 녹는점은 매우 다양합니다. 예를 들어 수은은 상온에서 액체이지만, 텅스텐은 3000도가 넘어야 녹습니다. 이는 금속의 종류와 자유전자의 수, 원자 크기 등 여러 요인이 복합적으로 작용하기 때문입니다.
많은 학생들이 “어떤 결합이 가장 강한가요?”라고 묻곤 합니다. 사실 이 질문에는 정답이 없습니다. 물질마다 결합의 세기가 다르기 때문이죠. 다이아몬드의 공유결합은 엄청나게 강하지만, 요오드 분자(I2)의 공유결합은 상대적으로 약합니다. 마찬가지로 산화마그네슘(MgO)의 이온결합은 매우 강하지만, 요오드화은(AgI)의 이온결합은 비교적 약합니다.
6. 일상생활에서 만나는 화학결합의 예시들
우리 주변을 둘러보면 세 가지 화학결합의 예를 쉽게 찾을 수 있습니다. 아침에 일어나서 양치질할 때 사용하는 치약에는 불소 화합물이 들어있는데, 이는 이온결합 물질입니다. 치약의 계면활성제는 공유결합으로 이루어진 유기 화합물이고, 칫솔대가 금속이라면 금속결합 물질이겠죠.
주방에서도 화학결합의 향연을 볼 수 있습니다. 요리할 때 사용하는 소금(NaCl)과 베이킹소다(NaHCO3)는 이온결합 물질입니다. 설탕(C12H22O11)과 식초의 주성분인 아세트산(CH3COOH)은 공유결합 물질이고, 스테인리스 냄비와 알루미늄 호일은 금속결합 물질입니다. 각각의 결합 특성 때문에 소금은 물에 잘 녹아 짠맛을 내고, 설탕은 달콤한 맛을 내며, 금속 조리기구는 열을 잘 전달합니다.
스마트폰도 화학결합의 종합 선물 세트입니다. 화면의 유리는 규소와 산소의 공유결합으로 이루어져 있고, 배터리 내부의 리튬 이온은 이온결합과 관련이 있으며, 내부 회로의 구리 배선은 금속결합으로 연결되어 있습니다. 각 부품이 제 역할을 할 수 있는 것은 각각의 화학결합이 가진 특성 덕분입니다.
건축물에서도 마찬가지입니다. 콘크리트에 들어가는 시멘트는 복잡한 이온결합 화합물들의 혼합물이고, 철근은 금속결합으로 이루어진 철로 만들어집니다. 창문의 유리는 공유결합 물질이고, 단열재로 사용되는 스티로폼은 공유결합으로 이루어진 고분자 물질입니다. 이렇게 각기 다른 결합의 물질들이 조화를 이루어 안전하고 편안한 건물을 만드는 것입니다.
의약품에서도 화학결합은 중요한 역할을 합니다. 아스피린 같은 진통제는 공유결합으로 이루어진 유기 화합물이고, 제산제에 들어가는 수산화마그네슘은 이온결합 물질입니다. 치과에서 사용하는 아말감은 수은과 다른 금속들의 금속결합으로 이루어져 있죠. 각각의 결합 특성이 약물의 효과와 체내 흡수에 영향을 미칩니다.
7. 결론 – 우리 주변의 모든 것이 화학결합의 결과물
지금까지 이온결합, 공유결합, 금속결합에 대해 자세히 알아보았습니다. 처음에는 복잡하고 어려워 보일 수 있지만, 원자들이 안정한 전자 배치를 이루려는 간단한 원리에서 시작된다는 것을 기억하면 됩니다. 마치 사람들이 행복하고 안정된 삶을 추구하듯이, 원자들도 가장 안정한 상태를 찾아가는 것이죠.
이온결합은 전자를 완전히 주고받는 극단적인 방식으로, 공유결합은 전자를 나누는 협력적인 방식으로, 금속결합은 전자를 공동체가 공유하는 방식으로 안정성을 추구합니다. 각각의 방식이 만들어내는 물질들은 저마다 독특한 성질을 가지며, 우리 삶을 풍요롭게 만들어줍니다.
화학결합을 이해하면 우리 주변 세계를 보는 눈이 달라집니다. 왜 다이아몬드가 그렇게 단단한지, 왜 소금물이 전기를 통하는지, 왜 금속이 구부러지면서도 부서지지 않는지 이해할 수 있게 됩니다. 더 나아가 새로운 물질을 설계하고 만들어내는 데도 이런 지식이 활용됩니다. 반도체, 신소재, 의약품 개발 등 현대 과학기술의 거의 모든 분야가 화학결합의 원리를 바탕으로 발전하고 있습니다.
학생 여러분들께 드리고 싶은 말씀은, 화학결합을 단순히 시험을 위해 외워야 하는 지식으로만 생각하지 말라는 것입니다. 여러분이 숨 쉬는 공기, 마시는 물, 먹는 음식, 입는 옷, 사용하는 스마트폰 등 모든 것이 화학결합의 결과물입니다. 이런 관점에서 보면 화학은 더 이상 교과서 속의 딱딱한 학문이 아니라, 우리 삶과 직접 연결된 살아있는 지식이 됩니다.
앞으로 소금을 뿌릴 때, 반지를 낄 때, 플라스틱 용기를 사용할 때, 잠시 멈춰서 그 안에 숨어있는 화학결합의 비밀을 떠올려보세요. 원자들이 어떻게 손을 잡고 있는지, 전자들이 어떻게 움직이고 있는지 상상해보세요. 그러면 평범해 보이던 일상이 조금은 특별하게 느껴질 것입니다.
화학결합의 세계는 아직도 많은 비밀을 품고 있습니다. 과학자들은 더 강하고, 더 가볍고, 더 유용한 새로운 물질을 만들기 위해 끊임없이 연구하고 있습니다. 어쩌면 이 글을 읽는 여러분 중에서 미래의 노벨 화학상 수상자가 나올지도 모릅니다. 화학결합의 원리를 완전히 새롭게 해석하거나, 지금까지 없던 결합 방식을 발견할 수도 있겠죠.
마지막으로, 화학결합은 단순히 원자들 사이의 결합만을 의미하는 것이 아닙니다. 그것은 우주의 모든 물질이 어떻게 형성되고 존재하는지를 설명하는 근본 원리입니다. 별에서 만들어진 원소들이 지구로 와서 화학결합을 통해 생명체를 이루고, 그 생명체 중 하나인 우리가 다시 화학결합을 연구하고 이해하려 한다는 것, 참으로 경이로운 일이 아닐까요?
이제 여러분도 이온결합, 공유결합, 금속결합의 차이를 명확히 이해하셨을 것입니다. 이 지식이 단순한 암기가 아닌, 세상을 이해하는 도구가 되기를 바랍니다. 화학의 눈으로 세상을 보면, 모든 것이 새롭고 흥미롭게 보일 것입니다. 오늘도 원자들은 여러분 주변에서 열심히 결합하고 있답니다!
출처
- Chemistry Learner – Ionic, Covalent, and Metallic Bonds (2023)
- Unacademy – Difference between Ionic, Covalent and Metallic bonds (2024)
- BYJU’S – Difference Between Ionic, Covalent and Metallic bonds (2022)
- Vedantu – Difference Between Ionic, Covalent and Metallic Bonds (2023)
- Study Mind – What is the difference between ionic, covalent and metallic bonding? (2023)
- JoVE – Chemical Bonding: Ionic, Covalent and Metallic Bonds (2025)
- Chemistry LibreTexts – The Bonding Spectrum (2020)
- 위키백과 – 화학 결합, 이온 결합